天津大学医学部卫生应急学院龚燕华教授团队发现创伤后急性肾损伤泛凋亡通路治疗新靶点
2026-02-12
天津大学医学部卫生应急学院龚燕华教授团队发现创伤后急性肾损伤泛凋亡通路治疗新靶点
近日,我院龚燕华教授团队发现创伤后横纹肌溶解相关急性肾损伤的泛凋亡(PANoptosis)通路治疗新靶点——RIG-I,并阐述了RIG-I作为蛋白质类DAMPs传感器分子组织新型RIGI-泛凋亡小体的关键机制。该研究发表在生物医药领域的国际权威跨学科期刊、美国转化医学学会的官方期刊《Translational Research》上(创刊至今111年历史)。题为:“Targeting RIG-I alleviates renal tubular epithelial cells PANoptosis during post-traumatic rhabdomyolysis”。

灾难事故背后的“沉默杀手”:创伤后横纹肌溶解与急性肾损伤
在大型地震、泥石流、车祸等灾难事故中,创伤后机体受挤压和冲击造成的横纹肌溶解是威胁伤员生命的“隐形杀手”。肢体肌肉组织遭受挤压、缺血等损伤后,大量肌红蛋白(Mb)从破损肌细胞中释放进入血液循环,超过了肾小球滤过能力在肾脏累积,引发创伤后横纹肌溶解相关急性肾损伤,又称挤压综合征相关性急性肾损伤(CS-AKI)。数据显示,即使接受透析治疗,CS-AKI患者死亡率仍高达21%,而目前临床缺乏针对肾性AKI的有效治疗手段,这也是应急医学亟待突破的。
Mb沉积在肾小管中引起的肾小管上皮细胞(TECs)的大量死亡和炎症反应是导致肾性AKI的核心致病环节。过往关于TECs细胞死亡的研究主要集中在细胞凋亡、细胞焦亡或坏死性凋亡等单一途径,但细胞死亡领域的最新研究揭示了一种更复杂的机制——泛凋亡(PANoptosis)。这是一种新型程序性细胞死亡,受到泛凋亡小体(PANoptosome)的调控,具有细胞焦亡、细胞凋亡和坏死性凋亡的关键特征,但却不能被三种细胞死亡方式的任意一种单独表征。
重要机制发现:RIG-I PANoptosis的“总开关”与关键靶点
本研究首次发现维甲酸诱导基因I(RIG-I)是CS-AKI中TECs发生PANoptosis的“顶端传感器”,干扰RIG-I的表达可以缓解CS-AKI模型中的肾脏损伤。先前关于RIG-I的研究集中在先天免疫系统中识别病毒的模式识别受体,而本研究揭示其在非感染性疾病-严重创伤相关的器官损伤中也扮演关键角色:
1. 感知危险信号:Mb作为“损伤相关分子模式(DAMPs)”,被模式识别受体RIG-I识别并激活下游信号通路。
2. 组装泛凋亡小体:RIG-I与Mb、ASC、caspase-1、caspase-8、FADD、RIPK1、RIPK3等分子结合,形成新型“RIG-I PANoptosome”。
3. 触发级联反应:PANoptosome组装完成后,激活PANoptosis下游信号通路,导致TECs细胞死亡,释放炎症因子(如IL-1β、IL-18),加剧肾脏损伤。
4. 靶向干预:敲低/敲除RIG-I后,TECs中PANoptosis相关分子(如GSDMD-N、cleaved-PARP、p-MLKL)表达显著降低,RIG-I与PANoptosis关键分子的相互作用消失,细胞死亡率下降,肾脏损伤标志物(Kim-1、NGAL)表达也明显降低。即与单独抑制下游细胞凋亡、细胞焦亡或坏死性凋亡通路相比,敲除RIG-I能更显著提高细胞活力,提示其作为“上游总开关”的独特优势。
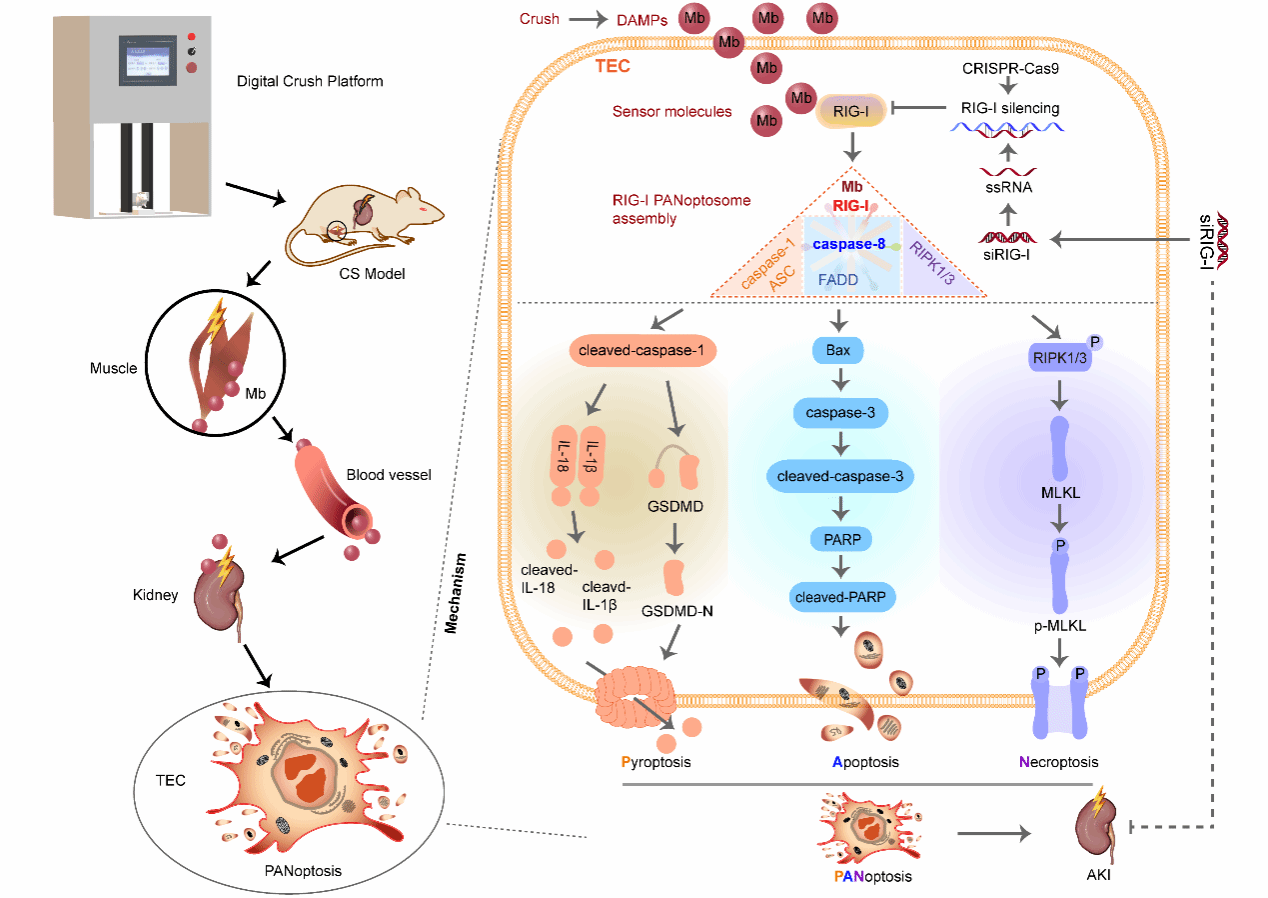
图1 CS-AKI中泛凋亡的发生机制及靶向治疗
从基础研究到应急医学临床转化:为创伤后急性肾损伤提供全新治疗方向
在应急医学的灾难事故救援实践以及创伤治疗的临床中,肾脏保护一直以来都是一场极为艰难且关键的“攻坚战”。肾脏作为泌尿系统的核心实质性器官,在各种复杂的情况下极易受到损害,而这种损害往往会给患者的健康带来严重威胁。本研究所发现的RIG-I-泛凋亡通路可作为CS-AKI的治疗靶点这一重要成果,为破解CS-AKI这一棘手难题带来了全新的希望。
1. 靶向RIG-I的救治方式:通过抑制RIG-I表达或阻断其与Mb的结合,可能从源头阻止PANoptosome组装,有效避免TECs过度死亡,减轻AKI。
2. 突破传统救治的局限性:传统治疗如补液、透析等对症治疗方式仅能缓解症状,而靶向RIG-I有望直击病理核心,为CS-AKI提供“治本”方案。
3. 拓展应用场景:除应急医学中的创伤后横纹肌溶解外,RIG-I可能在其他肌红蛋白相关疾病(如急性心肌梗死、不当运动导致的肌肉损伤等)中发挥作用,为多领域研究提供新思路。
在未来的应急医学临床转化研究进程中,通过针对RIG-I进行靶向干预的方式,比如课题组现正在国家自然科学基金等项目资助下研究RIG-I特异拮抗肽,有望“一石三鸟”高效阻止细胞凋亡、细胞焦亡或坏死性凋亡三条信号通路引发的TECs大量死亡,发挥肾脏保护作用,让更多的与此相关的患者能够远离AKI的风险,提高他们的生存质量以及康复的可能性。
天津大学医学部卫生应急学院讲师李宁博士为第一作者,博士研究生王俣汝、博士研究生乔欧、硕士研究生郝和睿为本文的共同第一作者。天津大学医学部卫生应急学院龚燕华教授、天津大学医学部药物科学与技术学院刘子川研究员为论文的共同通讯作者,天津大学医学部卫生应急学院为本论文的第一通讯单位。该研究主要得到了国家青年科学基金项目(C类)(No. 82504898,李宁)、国家自然科学基金面上项目(No. 82273998,龚燕华)的支持。课题组致力于应急医学领域生物治疗与新药创制研究,欢迎各类学生入组就读与交流。
原文链接:https://doi.org/10.1016/j.trsl.2026.02.002
内容来源:李宁、王俣汝
编辑:郭嘉懿


